
Nickel(II) carbonat
| Nickel(II) carbonat | |
|---|---|
 Mẫu niken(II) cacbonat
| |
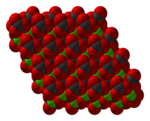 Cấu trúc của niken(II) cacbonat giống calci cacbonat
| |
| Danh pháp IUPAC | Niken(II) cacbonat |
| Tên khác | Niken(II) cacbonat(IV) Niken cacbonat Niken cacbonat(IV) Niken monocacbonat Niken monocacbonat(IV) Nikenơ cacbonat Nikenơ monocacbonat Nikenơ cacbonat(IV) Nikenơ monocacbonat(IV) |
| Nhận dạng | |
| Số CAS | 3333-67-3 |
| PubChem | 18746 |
| Số EINECS | 222-068-2 |
| Số RTECS | QR6200000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | 17701 |
| Thuộc tính | |
| Công thức phân tử | NiCO3 |
| Khối lượng mol | 118,9722 g/mol (khan) 191,03332 g/mol (4 nước) 227,06388 g/mool (6 nước) |
| Bề ngoài | bột màu xanh lá cây sáng |
| Khối lượng riêng | 4,39 g/cm³ |
| Điểm nóng chảy | 205 °C (478 K; 401 °F) phân hủy |
| Điểm sôi | |
| Độ hòa tan trong nước | 9,3 mg/100 mL |
| Tích số tan, Ksp | 6,6×10-9 |
| Cấu trúc | |
| Cấu trúc tinh thể | Trực thoi |
| Các nguy hiểm | |
| NFPA 704 |
|
| LD50 | 840 mg/kg |
| Ký hiệu GHS |
 
|
| Báo hiệu GHS | Danger |
| Chỉ dẫn nguy hiểm GHS | H302, H312, H315, H317, H319, H332, H334, H335, H350 |
| Chỉ dẫn phòng ngừa GHS | P201, P261, P280, P305+P351+P338, P308+P313 |
| Các hợp chất liên quan | |
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Niken(II) cacbonat là một hoặc một hỗn hợp của các hợp chất vô cơ chứa niken và cacbonat. Từ quan điểm công nghiệp, niken cacbonat quan trọng nhất là niken cacbonat base kiềm với công thức Ni4CO3(OH)6(H2O)4 (hay NiCO3·3Ni(OH)2·4H2O). Cacbonat đơn giản và dễ gặp nhất trong phòng thí nghiệm là NiCO3 và hexahydrat. Tất cả đều là chất rắn xanh thuận từ có chứa cation Ni2+. Cacbonat kiềm là một chất trung gian trong việc thanh lọc niken từ hydrocarbon của nó và được sử dụng trong mạ niken.
Cấu trúc và phản ứng
NiCO3 có cấu trúc như calcit, niken trong đó có cấu trúc bát diện.
Niken(II) cacbonat bị thủy phân khi tiếp xúc với các axit lỏng để tạo ra các dung dịch chứa ion [Ni(H2O)6]2+, giải phóng nước và carbon dioxide trong quá trình này. Nung niken(II) cacbonat sẽ thu được niken(II) oxit:
- NiCO3 → NiO + CO2↑
Niken(II) cacbonat kiềm có thể được tạo ra bằng cách xử lý dung dịch niken(II) sunfat với natri cacbonat:
- 4Ni2+ + CO32− + 6OH− + 4H2O → Ni4CO3(OH)6(H2O)4
Các hydrat cacbonat đã được điều chế bằng phương pháp điện phân niken với sự có mặt của carbon dioxide:
- 2Ni + 2O2 + 2CO2 + 12H2O → NiCO3(H2O)4
Hợp chất khác
- NiCO3 còn tạo ra một số hợp chất với NH3, như NiCO3·5NH3·4H2O. Tuy nhiên, chất rắn màu tím này không ổn định và dễ thủy phân thành 2NiCO3·3NH3 – chất rắn màu lục hay NiCO3·½NH3 cũng có màu tương tự. Ở mức NH3 hóa cao hơn có thể tạo NiCO3·6NH3 là chất rắn màu xanh dương, tan trong nước.
- NiCO3 còn tạo ra một số hợp chất với N2H4, như NiCO3·2N2H4·0,25H2O là chất rắn màu hồng hay NiCO3·3N2H4 là chất rắn màu hoa hồng nhạt, có tính nổ.
- NiCO3 còn tạo một số hợp chất với NH2OH, như NiCO3·2NH2OH có màu xanh dương đậm trong dung dịch.
Ứng dụng
Niken(II) cacbonat được sử dụng trong một số ứng dụng để làm gốm sứ và như là tiền thân của chất xúc tác.
An toàn
Nó hơi độc và gây kích ứng nhẹ. Tránh tiếp xúc kéo dài.
