Niraparib
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Zejula |
| Đồng nghĩa | MK-4827 |
| AHFS/Drugs.com | entry |
| Dược đồ sử dụng | By mouth |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 73% |
| Liên kết protein huyết tương | 83% |
| Chuyển hóa dược phẩm | Carboxylesterases |
| Chất chuyển hóa | M1 (carboxylic acid) |
| Chu kỳ bán rã sinh học | 36 hours |
| Bài tiết | 48% urine, 29% feces |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider |
|
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.210.548 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C19H20N4O |
| Khối lượng phân tử | 320.394 g/mol |
| Mẫu 3D (Jmol) | |
| Độ hòa tan trong nước | 0.7–1.1 mg/mL (20 °C) |
SMILES
| |
Định danh hóa học quốc tế
| |
Niraparib (tên thương mại Zejula) là một chất ức chế PARP phân tử nhỏ hoạt động bằng miệng do Tesaro phát triển để điều trị ung thư buồng trứng.
Niraparib đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cấp giấy phép theo dõi nhanh, và Tesaro đã nộp đơn đăng ký thuốc mới vào năm 2016. Nó đã được phê duyệt vào ngày 27 tháng 3 năm 2017 tại Hoa Kỳ, và đã được phê duyệt ở Châu Âu vào ngày 16 tháng 11 năm 2017 .
Sử dụng trong y tế
Thuốc được FDA Hoa Kỳ chấp thuận để điều trị duy trì cho bệnh nhân trưởng thành bị tái phát biểu mô buồng trứng, ống dẫn trứng hoặc ung thư phúc mạc nguyên phát, đáp ứng hoàn toàn hoặc một phần với hóa trị liệu dựa trên bạch kim.
Trong một nghiên cứu với 553 bệnh nhân, tỷ lệ sống không tiến triển (PFS) đối với những bệnh nhân bị đột biến BRCA nguy hiểm hoặc nghi ngờ trong mầm bệnh là 21,0 tháng khi điều trị bằng niraparib, so với 5,5 tháng khi dùng giả dược. Bệnh nhân không có đột biến như vậy có PFS là 9,3 tháng dưới niraparib so với 3,9 tháng dưới giả dược.
Chống chỉ định
Không có chống chỉ định được liệt kê trong thông tin kê đơn.
Tác dụng phụ
Các tác dụng phụ phổ biến nhất trong các nghiên cứu là số lượng tế bào máu thấp, cụ thể là giảm tiểu cầu (ở 61% bệnh nhân, nặng 29%), thiếu máu (50%, nặng 25%) và giảm bạch cầu trung tính (30%, nặng 20%). Các tác dụng phụ khác, chủ yếu từ nhẹ đến trung bình bao gồm buồn nôn, mệt mỏi và táo bón. Trong một nghiên cứu kéo dài hơn 250 ngày (trung vị), 15% bệnh nhân đã phải ngừng sử dụng niraparib vĩnh viễn do tác dụng phụ.
Tương tác
Không có nghiên cứu tương tác lâm sàng đã được thực hiện. Khả năng tương tác với các thuốc khác là thấp vì niraparib và chất chuyển hóa chính của nó không tương tác đáng kể với bất kỳ enzyme gan cytochrom P450 quan trọng nào trong ống nghiệm. Niraparib, nhưng không phải là M1, được vận chuyển bởi P-glycoprotein và BCRP, nhưng không ức chế đáng kể chúng. Cả niraparib và M1 đều không tương tác đáng kể với bất kỳ protein vận chuyển quan trọng nào khác.
Dược lý
Cơ chế hoạt động
Niraparib là chất ức chế enzyme PARP1 và PARP2.
Dược động học
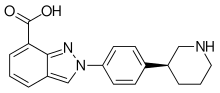
73% niraparib ăn vào được hấp thu trong ruột, và nó đạt nồng độ trong huyết tương cao nhất sau khoảng ba giờ, không phụ thuộc vào thức ăn. Trong tuần hoàn, 83% chất được liên kết với protein huyết tương. Nó bị bất hoạt bởi carboxylesterase thành chất chuyển hóa chính M1, dẫn xuất của axit cacboxylic, sau đó được glucuronid hóa.
Thời gian bán hủy sinh học trung bình là 36 giờ. 47,5% chất được tìm thấy trong nước tiểu và 38,8% trong phân. Niraparib không được chuyển hóa chiếm 11% trong nước tiểu và 19% trong phân.
Hóa học
Thuốc được sử dụng dưới dạng muối niraparib tosylate monohydrate, có màu trắng đến tinh thể trắng, không hút ẩm.
Nghiên cứu
Một nghiên cứu năm 2012 trên một dòng tế bào cho thấy các chất ức chế PARP thể hiện tác dụng gây độc tế bào không chỉ dựa trên sự ức chế enzyme PARP của chúng, mà bằng cách bẫy PARP của chúng trên DNA bị hỏng và sức mạnh của hoạt động bẫy này đã được đặt hàng là niraparib >> olaparib >> veliparib.
